Your browser does not fully support modern features. Please upgrade for a smoother experience.
Please note this is an old version of this entry, which may differ significantly from the current revision.
Subjects:
Biochemistry & Molecular Biology
I microRNA (miRNA) sono regolatori chiave dell'espressione genica, controllando diversi processi biologici come lo sviluppo cellulare, la differenziazione, la proliferazione, il metabolismo e l'apoptosi. Sono ben note le relazioni tra l'espressione di miRNA e l'insorgenza e la progressione di diverse malattie, come tumori, malattie cardiovascolari e reumatiche e disturbi neurologici. Un approccio basato sulla nanotecnologia potrebbe abbinare la consegna e il rilevamento di miRNA per andare oltre la fase di prova del concetto.
- nano-microRNA
- biomarcatore nanotecnologico
- consegna
- detection
1. Introduzione
La diagnosi precoce e trattamenti efficaci sono fondamentali per l'eradicazione della malattia e la guarigione dei pazienti, nonché per la sopravvivenza e/o la qualità della vita. Il cancro è una delle patologie che possono beneficiare di entrambi gli approcci, come molte altre malattie. I microRNA (miRNA) rappresentano uno strumento emergente che potrebbe essere efficace nel rilevare o curare diverse condizioni. I miRNA sono oligoribonucleotidi endogeni a filamento singolo corti (18-25 nucleotidi) non codificanti, che sono relativamente stabili; sono secreti prevalentemente nelle vescicole o in un complesso con altre proteine. Il ruolo del MiRNA è legato alla regolazione di diversi processi biologici, come lo sviluppo cellulare, la differenziazione, la proliferazione, il metabolismo e l'apoptosi [ 1]. Regolano infatti l'espressione genica e le alterazioni dei loro livelli di espressione correlano con l'insorgenza e la progressione di diverse malattie, come tumori, malattie cardiovascolari e reumatiche e disturbi neurologici [ 2 , 3 , 4]. In condizioni patologiche, si osservano livelli di miRNA disregolati, ma la relazione tra livelli di miRNA disregolati e malattia non è semplice. Le attività oncogeniche o di soppressione del tumore dei miRNA dipendono da quali geni vengono attivati o inibiti attraverso la sovraregolazione o la sottoregolazione dell'espressione dei miRNA. Pertanto, per garantire una diagnosi sicura, l'identificazione dei miRNA tramite il profilo di espressione è fondamentale; questo perché l'alterazione dei livelli di espressione di un singolo miRNA non ha una potenza diagnostica sufficiente rispetto al multiplexing, cioè il rilevamento parallelo o simultaneo di più miRNA noti. Le attuali strategie di quantificazione presentano limiti e svantaggi. In generale, tutti i metodi di quantificazione sono divisi in due categorie: una che utilizza l'oligo-ibridazione diretta senza amplificazione dell'RNA del campione e l'altra che richiede l'amplificazione del campione. I metodi che non utilizzano l'amplificazione del campione richiederanno una quantità iniziale relativamente maggiore di RNA totale, mentre gli altri che richiedono l'amplificazione del campione, con variazioni esterne poiché gestiscono le imperfezioni, possono anche essere amplificati. La tecnologia oligo-microarray è relativamente a basso costo e prontamente disponibile; uno svantaggio di questo metodo è la sua scala, poiché l'array risultante sarà relativamente grande. In alternativa, l'uso della sintesi e della modifica chimica delle sonde di RNA è costoso e spesso richiede una grande quantità di RNA totale. Molti altri metodi e strumenti sono stati sviluppati per la profilazione dell'espressione di miRNA. Problemi come la sensibilità e la specificità sono stati affrontati attraverso varie strategie; tuttavia sono ancora molto costosi, poiché rispondono a una molteplicità di esigenze specifiche; un'adeguata dimensione del campione, quantità e velocità del campione; e la necessità di identificare nuovi miRNA può essere costosa. Pertanto, vi è un grande interesse nello sviluppo di metodi innovativi e gli approcci basati sulle nanotecnologie sono particolarmente ricercati. La nanotecnologia avrà un forte impatto sulla consegna e sulla diagnosi attraverso il miRNA, dimostrando che l'approccio appena sviluppato funziona su campioni del "mondo reale" in condizioni standardizzate. Lo stesso vale anche per il trasporto e la consegna di miRNA, poiché l'inibizione o il mimetismo dei miRNA sono strategie attualmente in fase di valutazione per mantenere il livello di miRNA all'interno delle cellule,
In questa recensione, sono stati analizzati entrambi gli approcci (rilevamento e trattamento) che utilizzano strategie basate sulla nanotecnologia, per evidenziare le tendenze attuali in questo promettente campo di applicazioni biomediche ( Figura 1 e Figura 2 ).
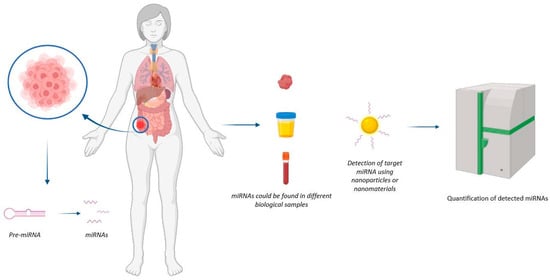
Figura 1. Rappresentazione del meccanismo d'azione dei nanodispositivi per il rilevamento di miRNA. Il nanodispositivo può rilevare il miRNA di interesse nel sito del tumore.
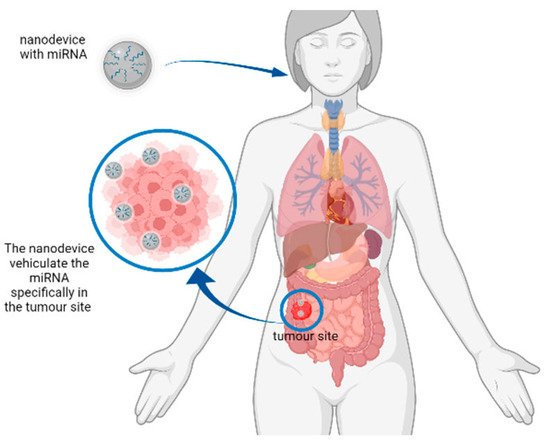
Figura 2. Rappresentazione di un ipotetico meccanismo d'azione di nanodispositivi per la consegna di miRNA. Il nanodispositivo può fornire il miRNA di interesse al sito del tumore per ridurre l'espressione dei geni correlati al tumore.
2. Rilevamento e biorilevamento di MiRNA
Convenzionalmente, il rilevamento dei miRNA si basa sulla reazione a catena della polimerasi in tempo reale (qRT-PCR), sui microarray, sul Northern blotting e sul sequenziamento di nuova generazione (NGS). Questi metodi di misurazione riflettono solo il livello medio di espressione genica e non possono fornire l'eterogeneità e le variazioni spaziotemporali transitorie dei miRNA nelle cellule viventi [ 5 ]. La principale differenza tra i metodi basati sulla nanotecnologia e quelli convenzionali risiede nel meccanismo di trasduzione. Le peculiari proprietà fisico-chimiche dei materiali nanostrutturati sono essenziali per migliorare la lettura del segnale [ 6]. Diverse nanoparticelle (NP) hanno eccellenti proprietà ottiche, che le rendono ideali per lo sviluppo di strategie di rilevamento. Alcuni NP sono emettitori di fluorescenza luminosi e stabili, come i nanocluster d'argento (AgNC) e i punti quantici (QD), e possono essere utilizzati direttamente o in strategie di trasferimento di energia di risonanza di fluorescenza. Altre NP, come le NP d'oro (AuNP) e le NP carboniose, possono essere utilizzate come efficienti quencher di fluorescenza negli approcci di recupero della fluorescenza. In presenza di miRNA bersaglio, i fluorofori, rilasciati fisicamente o chimicamente dalla NP, possono emettere fluorescenza in modo dipendente dalla concentrazione.
These few examples indicate that nanomaterials can have great potential in miRNA detection and biosensing. Biosensors represent innovative analytical tools for clinical diagnosis as well as for a better understanding of the molecular mechanisms involved in pathophysiology, revealing new biomarkers that are useful for the evaluation of appropriate pharmaceutical treatments [7]; moreover, miRNAs are surely promising and effective biomarkers. Biosensors can help in the early diagnosis and monitoring of pathological conditions, particularly for oncological diseases, and are useful in prognosis, surveilling the evolution of the disease, and opening the door to access to global health care. Among the different biosensing techniques, plasmonic sensor platforms are able to analyse different classes of biomolecules of clinical interest [8]. Different classes of biomolecules can be quantitatively detected in real time via high-throughput exploitation of (Localized) the surface plasmon resonance (SPR or LSPR) of metal nanoparticles and nanofilms, able to monitor and also perform label-free interactions. In fact, surface plasmons have been employed to enhance the surface sensitivity of different spectroscopic techniques, such as fluorescence and Raman scattering, applied to the detection of biomolecules. In the case of metal nanoparticles, LSP oscillations are responsible for the deep colors of their suspensions or sols, due to strong absorption bands in the ultraviolet–visible region, that are not present in the bulk material. The surface interaction of metal nanoparticles with biopolymers such as proteins, DNA, and RNA causes shifts in this resonance that can be used to detect and quantify their presence.
This entry is adapted from the peer-reviewed paper 10.3390/ijms23126836
This entry is offline, you can click here to edit this entry!
