Фармакогеномика - это исследование того, как геномный фон связан с лекарственной устойчивостью и как стратегия терапии может быть изменена для определенного человека для достижения пользы. Тестирование фармакогеномики (PGx) дает врачам прекрасную возможность принять правильное решение в отношении каждого нетривиального пациента, который не отвечает на терапию. Хотя фармакогеномика стала проявлять растущий интерес для рынка здравоохранения в течение последних пяти-десяти лет, точные механизмы, связывающие генетический полиморфизм и наблюдаемые реакции на лекарственную терапию, не всегда ясны. Следовательно, успех тестирования PGx зависит от способности врача стандартизировать полученные результаты для каждого конкретного пациента.Pharmacogenomics is a study of how the genome background is associated with drug resistance and how therapy strategy can be modified for a certain person to achieve benefit. The pharmacogenomics (PGx) testing becomes of great opportunity for physicians to make the proper decision regarding each non-trivial patient that does not respond to therapy. Although pharmacogenomics has become of growing interest to the healthcare market during the past five to ten years the exact mechanisms linking the genetic polymorphisms and observable responses to drug therapy are not always clear. Therefore, the success of PGx testing depends on the physician’s ability to understand the obtained results in a standardized way for each particular patient. The review aims to lead the reader through the general conception of PGx and related issues of PGx testing efficiency, personal data security, and health safety at a current clinical level.
- pharmacogenetics,pharmacogenetic test,personalized medicine,genetic polymorphism
1. Введение Introduction.
P4-medicine represents an actively developing field of modern medical science. The P4 conception is based on a personalized approach to human health (Personalization, Prediction, Prevention, and Participation). Modern diagnostic kits allow the identification of human metabolic characteristics at the molecular level, thus enabling the revelation of a personal, genetically determined predisposition to a disease or certain metabolic disorders in particular individuals [1]. Personalized medicine involves drug therapy to improve the patient’s condition and minimize any adverse effects, thus increasing the quality of life at both the individual and socioeconomic levels.
Pharmacogenetics goes back to 1959 when Vogel coined this term to designate severe adverse drug reactions in a small number of patients reported by the pharmacologists [2]. The adverse reactions, which followed the administration of primaquine, succinylcholine, and isoniazid, were anemia, apnea, and peripheral neuropathy, respectively [3,4].
Pharmacogenetics is purposed to study the response to the drug therapy depending on the genetic background. Response to drugs is frequently governed by genes encoding drug-metabolizing proteins, thus, regulating drug transformation, pharmacokinetics, and pharmacodynamics [5].
PGx may support the investigation of the effect of vitamins [6,7] and additives/supplements and, to some degree [8], homeopathic preparations. However, there is no strong evidence regarding the interaction between genes and vitamins/supplements/homeopathies.
The majority of the related assays in PGx are erroneous or misinterpreted due to biases in the design of the experiment, small sampling, small size of the population, and insufficient time of observation. So far, it is obligatory to provide more correct experiments and researches to observe the suggested effects, otherwise, most of the discussion about the possible influence of non-pharmacological compounds on the genome could be considered doubtful.
In clinical practice, a physician follows the national standards of specialized medical care, based on the evidence from fundamental research and clinical trials of drugs. However, to a greater extent, the therapy process remains a creative task [9].
In addition to adverse drug reactions, the body can demonstrate immunity and/or just partial response to the treatment [10]. Despite the underlying causes of drug resistance remain unclear; however, one can suppose that this is connected with genetic factors. Moreover, aside from the predisposition to diseases, various body metabolic functions are also determined genetically. Namely, genetic variations probably determine the rates of synthesis and decay of multiple biomolecules in the body, the effect of pharmaceuticals, the metabolism of nutrients, etc. [11]. However, answers to these questions have not yet been received.
P4-медицина представляет собой активно развивающееся направление современной медицинской науки. Концепция P4 основана на индивидуальном подходе к здоровью человека (персонализация, прогнозирование, предотвращение и участие). Современные диагностические наборы позволяют идентифицировать метаболические характеристики человека на молекулярном уровне, что позволяет выявить личную, генетически детерминированную предрасположенность к заболеванию или определенным метаболическим нарушениям у конкретных людей [ 1 ]. Персонализированная медицина включает медикаментозную терапию для улучшения состояния пациента и сведения к минимуму любых побочных эффектов, тем самым повышая качество жизни как на индивидуальном, так и на социально-экономическом уровнях.Nevertheless, genetic testing is slowly finding its niche in drug therapy selection—this process is followed by improving care to a widening range of patients. Pharmacogenomic Biomarkers in Drug Labeling Food and Drug Administration (FDA) provides data about 297 drugs for 100 molecular biomarkers (www.fda.gov/drugs/science-and-research-drugs/table-pharmacogenomic-biomarkers-drug-labeling). Several companies offer genetic testing for adverse drug reactions in patients.
Фармакогенетика восходит к 1959 году, когда Фогель ввел этот термин для обозначения тяжелых побочных реакций на лекарства у небольшого числа пациентов, о которых сообщили фармакологи [ 2 ]. Побочными реакциями, которые возникли после приема примахина, сукцинилхолина и изониазида, были анемия, апноэ и периферическая невропатия соответственно [ 3 , 4 ].
Prospects for the Introduction of a Pharmacogenetic Test into the Clinic.
Фармакогенетика предназначена для изучения ответа на лекарственную терапию в зависимости от генетического фона. Ответ на лекарства часто регулируется генами, кодирующими белки, метаболизирующие лекарства, таким образом, регулируя трансформацию лекарства, фармакокинетику и фармакодинамику [ 5 ].Nowadays, personalized medicine becomes more and more important [18]. Ongoing clinical trials can result in the introduction of pharmacogenetic testing into practice. This may accelerate the approval of distinct medication with no obligation to be tested on a PGx matter, which makes their market entry faster and more cost-effective. Typically, genomic information related to individual patients is made available to those who prescribe therapy. By 2017, The UK planned to perform the sequencing of 100,000 genomes of cancer patients and patients suffering from occasional or most dangerous infectious diseases (HIV, hepatitis C, tuberculosis), and to provide the pharmacogenetic information about the patients admitted in the study by the National Health Service [19]. Company 23andMe (Sunnyvale, CA, USA) (www.23andme.com) also provides pharmacogenetic information to guide the treatment directly upon customer request [20]. The FDA approved the first pharmacogenetic test in 2005. That was AmpliChip CYP450 test system manufactured by Affymetrix (Santa Clara, CA, USA) and Third Wave Technologies (Madison, WI, USA) Invader UGT1A1 (UDP-glucuronosyltransferase) Molecular Assay. The approval procedure was endorsed by clinicians, general healthcare systems, insurance companies, and concerned patients to determine the best way to integrate these tests into clinical practice [21]. At the same time, the critical questions raised were as to whom the tests should be applied and what are the most appropriate circumstances for their application, what evidence is required for the application of these tests, and how the results of the tests must be stored in electronic health data depositaries [22]? Haga and Kantor [23] reviewed laboratories, which offer clinical PGx testing in the United States. Of the 111 reviewed laboratories, 76 offered PGx testing services. Of these laboratories, 31 laboratories offered tests for only specific genes; 30 laboratories offered tests for multiple genes, while only 15 laboratories offered both types of tests. A total of 45 laboratories offered 114 multigene panel tests that cover 295 genes. However, no clinical guidelines were available for most of these tests [23]. In the industry, there is a trend towards multiplex tests intended to detect polymorphisms in a large number of genes. In 2005, the FDA-approved AmpliChip test (Roche, Basel, Switzerland) was designed to analyze two genes [24]. In 2010, Affymetrix introduced the DMET chip to diagnose 225 genes; the latter number is now expanded to 231 genes [23,25]. In 2012, researchers from Stanford University and the University of Florida developed a panel containing an SNP array of 120 genes including 25 genes responsible for drug metabolism and 12 drug carrier genes [26]. In 2014, the PGRN-Seq capture test for the analysis of 84 pharmacogens was developed [27]. The variety of gene panels is not limited to the examples mentioned above. Other types of pharmacological tests are available or are under development [28,29].
PGx может способствовать исследованию эффекта витаминов [ 6 , 7 ] и добавок / добавок и, в некоторой степени [ 8 ], гомеопатических препаратов. Однако нет убедительных доказательств взаимодействия между генами и витаминами / добавками / гомеопатиями.Currently, the clinical relevance of multigene panels mainly depends on a few well-studied and classical genes. Using the 84 gene PGRN-Seq capture panel, the examination of only five genes among ca. 5000 patients indicated that 99% of tested patients carried at least one clinically valid variant or one known variant relevant to decide about their treatment [30]. However, the clinical significance of large multiplex panels can mainly be determined by a certain task to be solved. For instance, PGx testing can be arranged as an immediate decision on treatment based on a panel of genes with a high level of evidence for a particular drug. However, the most common type of multigenic complex panel PGx test without specific clinical indications can be performed for a forward-looking patient. Such tests can be warranted since alternative drugs can be further used, and the clinical relevance of the data can increase with time. Despite the absence of consensus on the preventive PGx testing [31,32], many healthcare organizations implemented such testing programs to obtain valuable information regarding clinical validity and usefulness [27,33].
Большинство связанных анализов PGx ошибочны или неверно истолкованы из-за предвзятости в дизайне эксперимента, небольшого размера выборки, небольшого размера популяции и недостаточного времени наблюдения
2. Пока что необходимы более точные эксперименты и исследования для наблюдения предполагаемых эффектов, в противном случае большинство дискуссий о возможном влиянии нефармакологических соединений на геном можно было бы считать сомнительными1. Audience for PGx Testing
Currently, PGx tests exist in various areas of medicine, including, but not limited to, psychiatry, cardiology, anesthesia, and oncology. Some clinical guidelines for PGx tests are accessible for the prediction of tricyclic antidepressants (TCAs) and selective serotonin reuptake inhibitor (SSRI) efficacy based on CYP2D6 and CYP2C19 activity [34,35]. Recent studies revealed reduced adverse effects and improved scores in depressed patients after PGx-based antidepressant therapy [36]. PGx testing is particularly attractive given the time frame required. For instance, the estimation of the complete therapeutic response to SSRIs can require 4 to 6 weeks [37]. The patient and the healthcare provider can spend several months adjusting the dose and/or prescribing new medications before it becomes clear that the therapy does not lead to the therapeutic effect. PGx testing can allow a physician to determine the best drug for a given situation in a much shorter time.
PGx testing applicability, to a certain extent, depends on the intensity of potential adverse reactions to the drug. For instance, Abacavir, used for HIV treatment, can produce severe cutaneous adverse reactions (SCAR) [38]. Generally, the risk is low, but HLA-B*57:01 variation is related to much more pronounced SCAR after Abacavir intake. Thus, this drug is contraindicated for HLA-B*57:01- positive patients [38].
The use of PGx testing is relevant to the selection of the Warfarin dose. Intake of dietary vitamin K, health and social conditions, and genetic variations were also found to affect Warfarin therapy [39]. Changes in CYP2C9 can disrupt the metabolism of Warfarin, and alterations in VKORC1 (vitamin K epoxide reductase) can increase the drug susceptibility of a patient [38,39].
The use of codeine was limited to adult patients after the evidence of a risk of increased adverse effects in pediatric patients. The study revealed adverse reactions in infants whose breastfeeding mothers underwent codeine therapy [40]. These reactions resulted from codeine conversion to morphine, performed mainly by CYP2D6 protein [41]. Similar reactions can occur with other CYP2D6-mediated pain relievers—such as tramadol, oxycodone, and hydrocodone [42].
The high interest of patients in PGx testing was revealed [43,44]. The patients are particularly interested in the possibility of using recommendations based on PGx test results to reduce adverse drug effects and to choose proper therapy [45]. However, the cost of the tests, the insurance coverage, and the availability of testing results represent the limitations for PGx testing [46,47]. Some questions are still relayed uncertain after PGx testing. Thus, patients should be appropriately informed about the capabilities of PGx testing [48].
For this reason, one should understand that PGx testing allows the identification of (1) drugs with an increased risk of causing adverse effects, (2) drugs with a narrow therapeutic index. Besides that, PGx testing can reduce the set of drugs for therapy and predict the drug dosage [48,49]. At the same time, PGx testing will not be efficient for predicting: (1) occurrence of all possible adverse reactions with a drug, (2) the risk of a specific adverse effect for all drugs, 3) the risk of occurrence of complications [49].
The PGx testing provides an opportunity in decision making of whether the chosen medication and treatment strategy is of advantage and gives the proper results over the expectations based on the obtained profile of patients. That is exactly what opens the door for personalized medicine, that is what should happen when a person has a choice: to be healed but not at a cost of health deterioration, not in awaiting while inappropriate drug boosts dire consequences instead of a satisfying outcome.
В клинической практике врач следует национальным стандартам специализированной медицинской помощи, основанным на данных фундаментальных исследований и клинических испытаний лекарств
2. Однако в большей степени терапевтический процесс остается творческой задачей [ 9 ]2. Choice of PGx Testing
PGx testing can be carried out either as a single gene analysis or as a multiplex panel of ten or more genes. Early testing mostly involves analyzing multiple variants of the same gene, targeting the most common and most effective variants. Novel technologies significantly increased the number of genes and variations covered by a single test. Most PGx tests analyze a variety of clinically relevant SNPs. During the determination of the best test or panel for a patient (or a population), one should consider the therapeutic indication. For instance, testing for CYP2D6 and CYP2C19 is required for antidepressant therapy. In addition, it will also be useful to consider whether the patient would benefit from a PGx test for cardiovascular and pain-killing drugs [58]. A panel test can be more expensive than a single gene assay, but it ensures that co-prescribed drugs are also tested.
Panel PGx tests are heterogeneous and vary in volume and scope [59,60]. Most of the panels cover several of the best-studied and most potent genes. The panel can contain SNP combinations based on a literature review of prospective studies. A panel that includes many genes may not necessarily provide additional value to the patient, as not all options offer the same clinical relevance. Some variants can be extremely rare outside of certain populations but can be quite common within a certain group. For instance, the HLA-B * 15: 02 variant, associated with an increased risk of SCAR in patients prescribed carbamazepine, has an allele frequency of 0.04% in patients of European descent and 6.88% in patients of East Asian descent [61]. A panel can be more beneficial to the patient if it analyzes options that match their ethnic origin more closely.
One should keep in mind available alternatives or special analyses. Multiple copies of the CYP2D6 gene (e.g., duplications) occur in about 1 in 8 patients, and this number may be even higher in black and Asian patients [62]. Gene duplication can cause increased enzymatic activity and can be clinically relevant. However, not all panels can reveal the presence or degree of gene duplication.
In addition to the panel contents, one should consider such factors as the type of biomaterial (buccal smear, saliva, or blood, etc.) since the way of biomaterial sampling can pose a problem for the patient. The access to results and the methods of their obtaining also represent the factors that should be considered. Several panels provide nothing but raw genetic data, while others are fully integrated into the electronic health record and enable sophisticated clinical decision support systems (CDS). Finally, one should consider the potential cost of PGx testing. Patients vary in ways and means to pay for testing.
Помимо побочных реакций на лекарства, организм может демонстрировать иммунитет и / или частичную реакцию на лечение [ 10 ]
2. Несмотря на то, что основные причины лекарственной устойчивости остаются неясными; однако можно предположить, что это связано с генетическими факторами3. Кроме того, помимо предрасположенности к заболеваниям, различные метаболические функции организма также определяются генетически Interpreting PGx Test Results
When prescribing PGx testing, one should keep in mind that the result obtained represents only a part of the overall picture of the patient’s condition. Therefore, to determine the therapy risks and benefits, the PGx test results should be used and interpreted by taking into account the state of all the patient’s systems, concomitant medications, and current pathological conditions. When the “best” drug is identified with the PGx test, this does not necessarily mean that it should be used in therapy since the patient may have a history of severe adverse reactions to the drug. Conversely, the PGx test identification of an increased risk of therapeutic failure should not lead to drug discontinuation if the current therapy is effective. Different result structures can be used, depending on the gene and protein in question [63]. Some genes can be described in terms of metabolic activity, some by their general function, and others only as present or absent. Several PGx test results describe general gene function—such as SLCO1B1 (solute carrier organic anion transporter family member 1B1), associated with simvastatin; VKORC1 (vitamin K epoxide reductase complex subunit 1), associated with Warfarin; OPRM1 (opioid receptor Mu 1), associated with opioids [63]. Results for these genes can be reported as normal, intermediate, or low function. For instance, a “normal gene function” result indicates that no change in the patient’s dosage regimen is required. In other cases (decreased or poor function), the physician’s recommendations will be based on the information on a reduced functional activity (or complete inactivity) of the analyzed genes.
PGx test results can be “positive” or “negative” [57]. For instance, human leukocyte antigen (HLA) genes produce essential components of the immune system. Patients who are positive for HLA-B * 58: 01, run an increased risk of hypersensitivity to allopurinol; patients, who are positive for HLA-B * 15: 02, run an increased risk of SCAR with carbamazepine or oxcarbazepine [64,65].
The way the results are presented can vary considerably from one report to another. The results can be delivered either as raw genetic data or as the ultimate therapeutic recommendation. In the reports, a proprietary iconography can be used for the description of results. This iconography can use specific symbols to indicate patients in which an increased risk of adverse effects or therapy ineffectiveness is expected. Other reports can use a traffic light view with three main drug categories: green for normal risk, yellow for use with caution, and red for exclusion. Results displayed in any format can cause the provider to oversimplify the PGx test results, ignoring additional clinical considerations.
Below (Fig. 1) is an example of an abbreviated PGx test performed by AyassBioScience
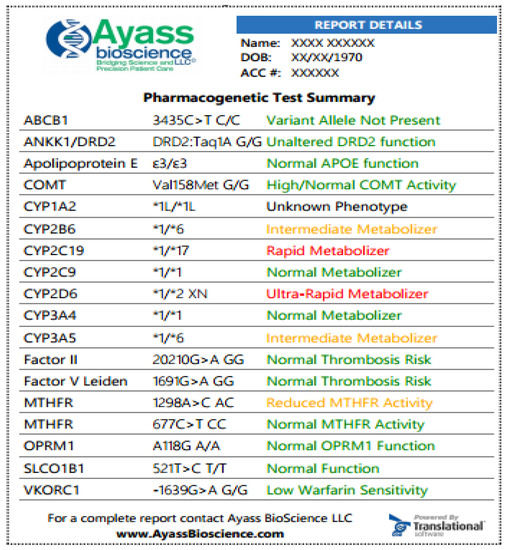
Fig. А именно, генетические вариации, вероятно, определяют скорость синтеза и распада множества биомолекул в организме, действие фармацевтических препаратов, метаболизм питательных веществ и т. Д. [ 11 ]. ОднакоSamples ответов на эти вопросы пока не получено.
Тем не менее, генетическое тестирование постепенно находит свою нишу при выборе лекарственной терапии - за этим процессом следует улучшение ухода за все более широким кругом пациентов. Фармакогеномные биомаркеры в маркировке лекарственных средств Управление по контролю за продуктами и лекарствами (FDof PGx test at A) предоставляет данные о 297 лекарствах для 100 молекулярных биомаркеров ( www.fdya.gov/drugs/science-and-research-drugs/table-pharmacogenomic-biomarkers-drug-labelingsBioScience: The report is featured with color-coded information for easier navigation ).and Несколько компаний предлагают генетические тесты на побочные эффекты у пациентовattention.
2. ПерспективыThe внедрения фармакогенетического теста в клинику.
Вgreed color indicates that the нашиmedication дни персонализированная медицина становится все более важной [ 18 ]. Продолжающиеся клинические испытания могут привести к внедрению фармакогенетических тестов в практику. Это может ускорить одобрение отдельных лекарств без обязательного тестирования на PGxcan be prescribed according to standard regimens, что сделает их выход на рынок более быстрым и экономичным. Обычно геномная информация, относящаяся к отдельным пациентам, предоставляется тем, кто назначает терапию. К 2017 году Великобритания планировала выполнить секвенирование 100000 геномов онкологических больных и пациентов, страдающих случайными или наиболее опасными инфекционными заболеваниями (ВИЧ, гепатит C, туберкулез), и предоставить фармакогенетическую информацию о пациентах, допущенных к исследованию. Национальная служба здравоохранения [ 19 ]. Компания 23andM the (Саннивейл, Калифорния, США) ( www.23arisk for the indmicate.comd condition )is также предоставляет фармакогенетическую информацию для руководства лечением непосредственно по запросу клиента [not increased; yellow color—indicated that dosage adjusting is required, there is an 20increased ].vigilance FDAor одобрило первый фармакогенетический тест в 2005 году. Это была тест-система AmpliChip CYP450, производимая Affymetrix (Санта-Клара, Калифорния, США) и Third Wave Technologies (Мэдисон, Висконсин, США). Молекулярный анализ Invader UGT1A1 (UDP-глюкуронозилтрансфераза).the patient has a moderate risk for the indicated condition; red color designates that medication has potentially reduced efficacy and Процедураincreased утверждения была одобрена клиницистами, общими системами здравоохранения, страховыми компаниями и заинтересованными пациентами, чтобы определить лучший способ интеграции этих тестов в клиническую практику [ 21 ]. В то же время были подняты критические вопросы о том, к кому следует применять тесты и каковы наиболее подходящие обстоятельства для их применения, какие доказательства требуются для применения этих тестов и как должны храниться результаты тестов. в электронных хранилищах медицинских данных [ 22 ]? Htoxicity or the patient has an increased risk for the indicagated и Kantor [ 23 ] провели обзор лабораторий, предлагающих клиническое тестирование PGx в Соединенных Штатахcondition. ИзIn 111 проверенных лабораторий 76 предлагали услуги тестирования PGx. Из этих лабораторий 31 лаборатория предлагала тесты только на определенные гены; 30 лабораторий предлагали тесты на множественные гены, и только 15 лабораторий предлагали оба типа тестов. В общей сложности 45 лабораторий предложили 114 мультигенных панельных тестов, охватывающих 295 генов. Однако для большинства этих тестов не было клинических руководств [ 23 ]. В отрасли существует тенденция к использованию мультиплексных тестов, предназначенных для обнаружения полиморфизмов в большом количестве генов. В 2005 году одобренный FDA тест Athe exempliChfip (Roche, Базель, Швейцария) был разработан для анализа двух генов [ 24 ]. В 2010 году ed results, the patient has a normal response to Affymetrpix представила чип DMET для диагностики 225 генов; последнее число теперь расширено до 231 гена [ 23 , 25 ]. В 2012 году исследователи из Стэнфордского университета и Университета Флориды разработали панель, содержащую массив SNP из 120 генов, включая 25 генов, ответственных за метаболизм лекарств, и 12 генов-носителей лекарств [ 26 ]. В 2014 г. был разработан тест захвата PGRN-Saban (the drug is a substrate for theq для анализа 84 фармакогенов [ 27 ]. Разнообразие генных панелей не ограничивается приведенными выше примерами. Доступны или разрабатываются другие виды фармакологических тестов [ 28 , 29 ].
В настоящее время клиническая значимость мультигенных панелей в основном зависит от нескольких хорошо изученных и классических генов. Используя панель захвата 84 генов PGRN-Seq, исследование только пяти генов из ок. 5000 пациентов указали, что 99% протестированных пациентов имеют по крайней мере один клинически валидный вариант или один известный вариант, имеющий значение для принятия решения о лечении [ 30 ]. Однако клиническое значение больших мультиплексных панелей во многом определяется определенной задачей, которую необходимо решить. Например, тестирование PGfflux можетtransport быть организовано как немедленное решение о лечении, основанное на группе генов с высоким уровнем доказательности для конкретного препарата. Однако наиболее распространенный тип мультигенного комплексного панельного proteins PGx-теста без конкретных клинических показаний может быть выполнен для перспективного пациента. Такие тесты могут быть оправданы, поскольку в дальнейшем могут использоваться альтернативные препараты, а клиническая значимость данных может возрасти соgp временем. Несмотря на отсутствие консенсуса в отношении профилактического тестирования PGx [ 31 , 32 ], многие медицинские организации внедрили такие программы тестирования, чтобы получить ценную информацию о клинической валидности и полезности [ 27 , 33 ].
3.1. Аудитория для тестирования PGx
В настоящее время тесты PGx существуют в различных областях медицины, включая, помимо прочего, психиатрию, кардиологию, анестезию и онкологию. Некоторые клинические руководства по тестам PGx доступны для прогнозирования эффективности трициклических антидепрессантов (ТЦА) и селективных ингибиторов обратного захвата серотонина (СИОЗС) на основе активности ABCYP2D6 и CYP2C19 [ 34 , 35 ]. Недавние исследования показали уменьшение побочных эффектов и улучшение показателей у пациентов с депрессией после терапии антидепрессантами на основе PGx [ 36 ]. Тестирование PGx особенно привлекательно с учетом необходимых временных рамок. Например, для оценки полного терапевтического ответа на СИОЗС может потребоваться от 4 до 6 недель [ 37 ]. Пациент и врач могут потратить несколько месяцев на корректировку дозы и / или назначение новых лекарств, прежде чем станет ясно, что терапия не приводит к терапевтическому эффекту. Тестирование PGx может позволить врачу определить лучший препарат для данной ситуации в гораздо более короткие сроки.
Применимость тестирования PGx в определенной степени зависит от интенсивности потенциальных побочных реакций на препарат. Например, абакавир, используемый для лечения ВИЧ, может вызывать серьезные кожные побочные реакции (SCARB1) [and 38 ]. В целом риск невелик, но вариация HLA-B * 57: 01 связана с гораздо более выраженным SCAR после приема абакавира. Таким образом, этот препарат противопоказан HLRP (A-B * 57: 01-положительным пациентам [ 38 ].
Использование теста PGx имеет отношение к выбору дозы варфарина. Было обнаружено, что потребление витамина К с пищей, состояние здоровья и социальные условия, а также генетические вариации также влияют на терапию варфарином [ 39 ]. Изменения в CYP2C9 могут нарушить метаболизм варфарина, а изменения в VKORC1 (эпоксидредуктаза витамина К) могут увеличить лекарственную восприимчивость пациента [ 38 , 39 ].
Использование кодеина было ограничено взрослыми пациентами после доказательства риска усиления побочных эффектов у педиатрических пациентов. В ходе исследования были выявлены побочные реакции у младенцев, кормящие матери которых получали терапию кодеином [ 40 ]. Эти реакции являются результатом превращения кодеина в морфин, осуществляемого в основном белком CYP2D6 [ 41 ]. Подобные реакции могут возникать с другими обезболивающими, опосредованными CYP2D6, такими как трамадол, оксикодон и гидрокодон [ 42 ].
Выявлен высокий интерес пациентов к тестированию PGx [ 43 , 44 ]. Пациентов особенно интересует возможность использования рекомендаций, основанных на результатах теста PGx, для уменьшения побочных эффектов лекарств и выбора правильной терапии [ 45 ]. Однако стоимость тестов, страховое покрытие и доступность результатов тестирования представляют собой ограничения для тестирования PGx [ 46 , 47 ]. Некоторые вопросы все еще остаются неопределенными после тестирования PGx. Таким образом, пациенты должны быть соответствующим образом проинформированы о возможностях тестирования PGx [ 48 ].
По этой причине следует понимать, что тестирование PGx позволяет идентифицировать (1) препараты с повышенным риском возникновения побочных эффектов, (2) препараты с узким терапевтическим индексом. Кроме тогоand, PGx-тестирование позволяет сократить набор препаратов для терапии и спрогнозировать дозировку препаратов [ 48 possibly, 49decreased ]. В то же время тестирование PGx не будет эффективным для прогнозирования: (1) возникновения всех возможных побочных реакций с лекарством, (2) риска специфического побочного эффекта для всех лекарств, 3) риска возникновения осложнений [ 49 ].
Тестирование PGx дает возможность принять решение о том, являются ли выбранные лекарства и стратегия лечения преимуществами и дает надлежащие результаты по сравнению с ожиданиями, основанными на полученном профиле пациентов. Это именно то, что открывает двери для персонализированной медицины, это то, что должно произойти, когда у человека есть выбор: выздороветь, но не за счет ухудшения здоровья, не в ожидании, пока неподходящий препарат вызовет ужасные последствия вместо удовлетворительного результата.
2.2. Ресурсы в фармакогенетическом секторе
Из-за постоянно меняющейся природы генетической медицины следует знать о дальнейших изменениях в рекомендациях по тестированию или интерпретации результатов. Эту задачу можно упростить, если использовать доступные на данный момент ресурсы Интернета ( таблица 1 ).
Таблица 1. Наиболее посещаемые и популярные интернет-ресурсы в фармакогенетическом секторе.
| Ресурс | Описание | Справка |
|---|---|---|
| Coursera | Интернет-курс персонализированной медицины, который включает короткие обучающие курсы по генетике и механизмам, определяющим вариабельность реакции на лекарства; разработка этических вопросов и возражений, связанных с внедрением и внедрением широкомасштабного секвенирования генома в клиническую практику. | https://www.coursera.org/learn/personalizedmed |
| CPIC | Международный консорциум, который специализируется на публикации руководств по лекарственным препаратам на основе генотипов, чтобы помочь клиницистам понять применимость доступных результатов генетических тестов для оптимизации лекарственной терапии. | https://www.cpicpgx.org [ 50 , 51 ] |
| eMERGE | Финансируется NIH. Эта сеть объединяет исследователей с широким спектром знаний в области геномики, статистики, этики, информатики и клинической медицины от ведущих медицинских исследовательских институтов по всей стране до исследований в области геномики, включая открытия, клиническое внедрение и общедоступные ресурсы. | https://www.emerge-network.org |
| GTR | Бесплатный ресурс, который предоставляет обобщенное хранилище исчерпывающей информации о генетических тестах, которое предоставляется и поддерживается поставщиками; Основная аудитория - клиницисты и исследователи. | https://www.ncbi.nlm.nih.gov/gtr [ 52 ] |
| ЗАЖИГАТЬ | Был разработан для расширения использования геномной медицины путем поддержки включения геномной информации в клиническую практику и изучения методов эффективного внедрения, распространения и устойчивости в различных клинических условиях. | https://www.gmkb.org |
| Мой геном наркотиков | Портал для изучения того, как генетика влияет на реакцию на лекарства и как результаты генетического тестирования могут быть применены в здравоохранении. | https://www.mydruggenome.org |
| ФармГКБ | Онлайновая база знаний, отвечающая за сбор, подбор, интеграцию и распространение данных о влиянии генетической изменчивости на реакцию человека на лекарства. | https://www.pharmgkb.org [ 53 ] |
CPIC - Консорциум по внедрению клинической фармакогенетики; responseMERGE - Сеть электронных медицинских записей и геномики; GTR - Реестр генетического тестирования; IGNITE - ГЕНОМИКА НА ПРАКТИКЕ; NIH - Национальные институты здоровья; Phato BuprmGKB - База фармакогенетических знанийopion.
Кроме того, известно меньше ресурсов, заслуживающих внимания. Среди них портал MayBupro Clpinic, на котором были опубликованы многочисленные образовательные материалы «AskMayoExpert» как для врачей, так и для пациентов с целью повышения общих знаний и практических навыков [ 54 ]. Детская исследовательская больница Сент-Джуда позволяет отслеживать интегрированную на веб-сайте информацию о генах или лекарствах, а также публикации и презентации по конкретным реализациям [ 55 ]. Компания Ubiquon is metabolized to itous Pharmacogenomics (U-PGx) разработала платформу электронного обучения для распространения общих знаний по фармакологии, подходящую для врачей и фармацевтов ( httactive metabolite hydroxybups://uropgx.eu/ion )by [ 56 ].
Поддержка и развитие этих ресурсов может быть ценным инструментом для изучения предстоящих или менее известных фармакогенетических взаимодействий. Несколько организаций в настоящее время обеспечивают интеграцию с программами PGx и обновляют текущие данные [ 51 , 57 ].
2.3. Выбор тестирования PGx
PGx-тестирование может проводиться либо как анализ одного гена, либо как мультиплексная панель из десяти или более генов. Раннее тестирование в основном включает в себя анализ нескольких вариантов одного и того же гена с нацеливанием на наиболее распространенные и наиболее эффективные варианты. Новые технологии значительно увеличили количество генов и вариаций, охватываемых одним тестом. Большинство тестов PGx анализируют множество клинически значимых SNP. При определении лучшего теста или панели для пациента (или популяции) следует учитывать терапевтические показания. Например, для антидепрессивной терапии требуется тестирование на CYP2D6 и CYP2C19. Кроме того, также будет полезно подумать о том, выиграет ли пациент от теста PGx на сердечно-сосудистые и обезболивающие [ 58 ]. Панельный тест может быть более дорогостоящим, чем анализ одного гена, но он гарантирует, что лекарства, назначенные совместно, также будут проверены.
Панельные тесты PGx неоднородны и различаются по объему и объему [ 59 , 60 ]. Большинство панелей охватывает несколько наиболее изученных и наиболее эффективных генов. Панель может содержать комбинации SNP на основе обзора литературы о проспективных исследованиях. Панель, включающая множество генов, не обязательно может представлять дополнительную ценность для пациента, поскольку не все варианты имеют одинаковую клиническую значимость. Некоторые варианты могут быть чрезвычайно редкими за пределами определенных популяций, но могут быть довольно распространены в определенной группе. Например, вариант HLA-B * 15: 02, связанный с повышенным риском SCAR у пациентов, прописанных карбамазепином, имеет частоту аллелей 0,04% у пациентов европейского происхождения и 6,88% у пациентов восточноазиатского происхождения [ 61 ]. ПанельThis может быть более полезной для пациента, если она будет более точно анализировать варианты, соответствующие их этническому происхождению.
Следует иметь в виду доступные альтернативы или специальные анализы. Множественные копии гена CYP2D6 (например, дупликации) встречаются примерно у 1 из 8 пациентов, и это число может быть еще выше у чернокожих и азиатских пациентов [ 62 ]. Дублирование генов может вызывать повышенную ферментативную активность и иметь клиническое значение. Однако не все панели могут выявить наличие или степень дупликации генов.
Помимо содержания панели, следует учитывать такие факторы, как тип биоматериала (буккальный мазок, слюна или кровь и т. Д.), Поскольку способ отбора биоматериала может представлять проблему для пациента. Доступ к результатам и методы их получения также представляют собой факторы, которые следует учитывать. Некоторые панели не предоставляют ничего, кроме сырых генетических данных, в то время как другие полностью интегрированы в электронную медицинскую карту и позволяют использовать сложные системы поддержки клинических решений (CDS). Наконец, следует учитывать потенциальную стоимость тестирования PGx. Пациенты различаются способами и способами оплаты тестирования.
2.4. Интерпретация результатов теста PGx
При назначении тестирования PGx следует иметь в виду, что полученный результат представляет собой лишь часть общей картины состояния пациента. Поэтому для определения рисков и преимуществ терапии следует использовать и интерпретировать результаты теста PGx с учетом состояния всех систем пациента, сопутствующих лекарств и текущих патологических состояний. Когда с помощью теста PGx определяется «лучший» препарат, это не обязательно означает, что его следует использовать в терапии, поскольку у пациента в анамнезе могут быть серьезные побочные реакции на препарат. И наоборот, выявление повышенного риска терапевтической неудачи с помощью теста PGx не должно приводить к отмене препарата, если текущая терапия эффективна. В зависимости от рассматриваемого гена и белка могут использоваться различные структуры результатов [ 63 ]. Некоторые гены можно описать с точки зрения метаболической активности, некоторые - по их общей функции, а другие - только как присутствующие или отсутствующие. Некоторые результаты тестов PGx описывают общую функцию гена, такого как SLCO1B1 (член семейства переносчиков органических анионов 1B1), связанного с симвастатином; VKORC1 (субъединица 1 комплекса эпоксидредуктазы витамина К), связанный с варфарином; OPRM1 (опиоидный рецептор Mu 1), связанный с опиоидами [ 63 ]. Результаты для этих генов могут быть представлены как нормальная, промежуточная или низкая функция. Например, результат «нормальная функция гена» указывает на то, что изменения режима дозирования пациента не требуется. В других случаях (снижение или плохая функция) рекомендации врача будут основываться на информации о сниженной функциональной активности (или полном бездействии) анализируемых генов.
Результаты теста PGx могут быть «положительными» или «отрицательными» [ 57 ]. Например, гены лейкоцитарного антигена человека (HLA) продуцируют важные компоненты иммунной системы. Пациенты с положительным результатом на HLA-B * 58: 01 имеют повышенный риск гиперчувствительности к аллопуринолу; Пациенты с положительным результатом на HLA-B * 15: 02 имеют повышенный риск SCAR при применении карбамазепина или окскарбазепина [ 64 , 65 ].
Способ представления результатов может значительно отличаться от одного отчета к другому. Результаты могут быть представлены либо в виде сырых генетических данных, либо в качестве окончательной терапевтической рекомендации. В отчетах для описания результатов может использоваться собственная иконография. В этой пиктограмме могут использоваться специальные символы для обозначения пациентов, у которых ожидается повышенный риск побочных эффектов или неэффективности терапии. В других отчетах можно использовать режим светофора с тремя основными категориями лекарств: зеленый для нормального риска, желтый для использования с осторожностью и красный для исключения. Результаты, отображаемые в любом формате, могут привести к тому, что поставщик чрезмерно упростит результаты теста PGx, игнорируя дополнительные клинические соображения.
Ниже ( рис. 3 ) приведен пример сокращенного теста PGx, выполненного AymetassBiboScience (Фриско, Техас, США). (полный отчет можно найти на lite contributes to the thterapeutps://ayassbioscience.com/wp-content/uploads/2020/02/PGX-Medical-ManagementPrint-Fit-on-Page.pdf )ic effects of bupropion when used as a smoking cessation agent or as an antidepressant.

Рис. 3.The Образцыpatient теста PGx в AyassBioScience: отчет снабжен цветной информацией для облегчения навигации и внимания. Жадный цвет говорит о том, что лекарство можно назначать по стандартным схемам, и риск указанного состояния не повышен; желтый цвет - указывает на то, что требуется корректировка дозировки, имеется повышенная бдительность или у пациента умеренный риск указанного состояния; красный цвет означает, что лекарство потенциально имеет пониженную эффективность и повышенную токсичность или что у пациента повышенный риск указанного состояния. В приведенных в качестве примеров результатах у пациента наблюдается нормальный ответ на апиксабан (препарат является субстратом для белков оттока P-ghas also increased response (ABCB1) и BCRP (ABCG2) и, возможно, сниженный ответ на бупропион. Бупропион метаболизируется до его активного метаболит гидроксибупропиона с помощью CYP2B6. Этот метаболит способствует терапевтическому эффекту бупропиона при использовании в качестве средства для прекращения курения или в качестве антидепрессанта. У пациента также усиливается реакция на кодеин, который превращается в его активный метаболит морфин с помощью CYP2D6. Поскольку этот пациент является сверхбыстрого метаболизатора (УМ) ожидается значительно повышенный уровень морфина, и пациент подвергается высокому риску токсичности при приеме кодеина.
В отчете можно использовать различные способы представления информации. Поскольку каждый способ отличается, нужно быть осторожным, чтобы обеспечить полное понимание значения каждой категоризации [ 49 ].
2.5. Инструменты автоматизации для интеграции тестирования PGx в клинику
Быстро развивающиеся новые технологии секвенирования ДНК позволяют быстро и эффективно определять геномные характеристики организмов. Основным результатом развития геномных и постгеномных технологий стало значительное расширение возможностей изучения генетической природы всего спектра заболеваний человека. Полногеномное ассоциативное исследование (GWAto Codeine, which is converted into its active metabolite morphine by CYP2D6. S)ince клинических образцов позволило собрать данные о генетическом составе конкретных групп (семей или популяций), чтобы разработать индивидуальный подход к лечению. В связи с этим на сегодняшний день особую актуальность приобретают исследования механизмов генетической предрасположенности к многофакторным заболеваниям и выявление конкретных генетических маркеров. Такие методы широко используются в мире и в России, где современные технологии секвенирования постепенно внедряются в медицинские исследования и медицинскую практику, чтобы олицетворять стратегию лечения.
Секвенирование следующего поколения (NGS) используется для углубленного (множественного) считывания генетического материала, что необходимо, например, для повторного секвенирования и сборки новых геномов (dthis patient is the ultra-rapid metabolizer (UM), a greatly increased morphine le novo), транскриптомов и эпигеномных исследований. Этот метод позволяет выявить редкие вариации и лучше понять генетическую функцию. Однако лавина новых данных также создаст проблемы для исследователей и клиницистов, давая множество «вариантов неизвестной важности» при отсутствии четких показаний [ 49 ]. Модификации CDS необходимы для обеспечения хранения и использования новой архитектуры данных и новых программ доступности данных. Это, в свою очередь, откроет значительные возможности в ближайшие годы. Некоторые системы здравоохранения используют инструменты CDS для интеграции данных тестов PGel is ex в процесс принятия клинических решений и предоставления информации конечным пользователям [ 66 ]. Системы CDS могут использоваться для введения лекарств высокого риска и предоставления автоматизированных рекомендацийpected, указывающих,and почему определенные модификации должны быть применены к выбранному лекарству или дозе.
В исследовании U-PGthe patient is at high risk of toxicity PREPARE были разработаны решения для сайтов с ограниченной инфраструктурой электронных медицинских карт. Карта «Safety-Cwhen taking code» является частью мобильного CDS, и с помощью кода быстрого ответа медицинский работник направляется на веб-сайт с рекомендациями по дозировке, адаптированными для пациента [ 67 ]ine. На этой карточке также представлен обзор наиболее важных результатов теста PGx со списком препаратов с существующими (известными) рекомендациями [ 68 ].
A variety of ways of presenting the information can be used in the report. Since each way is different, one should be careful to ensure a complete understanding of the meaning of each categorization [49].
Такие инструменты CDS будут необходимы, поскольку тесты PGx станут более распространенными из-за появления новых результатов и форматов тестов2. Можно также сосредоточиться на разработке ориентированных на пациента приложений и порталов, через которые пациент может взаимодействовать со своими поставщиками услуг и получать консультацию по результатам4.
Automation Tools for Integrating PGx Testing into the Clinic
Повышение осведомленности медицинских работников и пациентов может стимулировать использование PGx-тестирования. Следовательно, лаборатории будут корректировать объем и тип доступных клинических тестов PGx в зависимости от клинических требований. Ожидаемый рост разработки мультигенных панельных тестов PGx следует за достижениями в онкологии, микробиологии и других областях. Однако надлежащее клиническое использование таких тестов, по-видимому, более сложное, требующее поддержки и участия множества заинтересованных сторон.Rapidly developing new technologies of DNA sequencing enabled quick and efficient identification of the genomic characteristics of organisms. The main result of the genomic and post-genomic technologies development was a significant expansion of the capabilities to study the genetic nature of a whole spectrum of human diseases. A genome-wide association study (GWAS) of clinical samples generated data on the genetic makeup featured for the specific groups (families or populations) to elaborate a personalized treatment approach. In this regard, to date, the research into the mechanisms of genetic predisposition to multifactorial diseases and the identification of specific genetic markers are of particular relevance. Such methods are widely used internationally and in Russia, where modern sequencing technologies are gradually introduced into medical research and medical practice to personify the treatment strategy.
Next-generation sequencing (NGS) is used for in-depth (multiple) reading of genetic material, which is necessary, for instance, for re-sequencing and assembly of new genomes (de novo), transcriptome, and epigenomic studies. This method allows one to reveal rare variations and to understand the genetic function better. However, the avalanche of new data will also make problems for researchers and clinicians, giving many “options of unknown importance” in the absence of clear indications [49]. Modifications of CDS are required to ensure the storage and use of new data architecture and new data availability programs. This, in turn, will identify significant opportunities in the coming years. Several healthcare systems use CDS tools to integrate PGx test data into clinical decision-making and provide information to end-users [66]. CDS systems can be used to administer high-risk drugs and provide automated recommendations indicating why certain modifications should be applied to a selected drug or dose.
The U-PGx PREPARE study developed solutions for sites with limited electronic health record infrastructure. The “Safety-Code” card is part of a mobile CDS, and with a quick response code, a medical professional is directed to a website with dosing recommendations customized for the patient [67]. This card also provides an overview of the most relevant PGx test results with a list of drugs with existing (known) recommendations [68].
Such CDS tools will be necessary, as PGx tests become more common due to the emergence of new results and test formats. One can also focus on developing patient-centered applications and portals, through which the patient can interact with his or her service providers and receive a consultation based on outcomes.
The increase in providers’ and patients’ awareness can stimulate the use of PGx testing. Consequently, laboratories will adjust the scope and type of available clinical PGx tests based on clinical requirements. The expected increase in the development of multigene panel PGx tests follows the advances in oncology, microbiology, and other fields. However, the proper clinical use of such tests appears to be more involved, requiring the support and participation of multiple interested parties.
3. Conclusions
We are on the verge of a new era in human genetic analysis. Deciphering the human genome, together with the development of high-throughput genetic analysis methods, provided a unique opportunity for the identification of complex genetic changes, resulting in the development of new branches of pharmacy: pharmacogenetics and pharmacogenomics. The genomic profiling of patients became a new diagnostic tool, enabling personalized drug therapy with higher effectiveness and fewer adverse effects. The pharmacogenetic tests can help select a specific drug with a specific dosage and administration regime, which will meet the requirements for the treatment of a particular patient in a specific setting, allowing one to avoid time-consuming dose adjustment inevitably associated with adverse effects.
Although PGx testing represents a significant therapeutic advance, it is just a healthcare professional’s arsenal tool of the future, increasing therapy effectiveness. The technological breakthrough will never override a physician’s experience and logic. This is a small paradigm shift towards the personalization of treatment.
PGx testing development inevitably will stimulate the progress in methods of data storage and data analysis, which are required for the integration of modern information technologies into routine clinical practice. However, the improvement in digital technologies, the increase in the volume and accessibility of databases is not the only problem in integrating genetic testing into the healthcare continuum. This, in turn, requires changes in the interaction between an individual patient and the healthcare system since the ultimate goal is the patient’s recovery or control of the disease, regardless of what laboratory techniques and data analysis technologies are employed. In other words, the treatment should take into account both the patient’s requirements and the test results. Today pharmacogenetics is in its infancy. A large pool of experimental, but mostly pilot, studies in this area have been accumulated; however, this information can barely be classified as systemic, which makes it difficult to explain the observed correlations between the presence of polymorphisms of a separate gene and epigenetic factors, or the severity of the course of the disease/resistance to therapy. The authors do not aspect information on congenital/acquired polymorphisms, even for the genetically determined diseases, such as cardiovascular diseases and diabetes mellitus. So far, pharmacogenetics provides mosaic information related to the association between the response to drug therapy depending on the genetic background. The next stage is expected to be the research on a larger group of participants, study the contribution of epigenetic factors, and providing clinical guidelines for adjusting or selecting the therapy based on the personal characteristics of the patient. Nevertheless, the field of pharmacogenetics is being actively developed and discussed, and the current demand for end-products in medicine is unusually high. We expect that soon researchers find answers to many questions that are still controversial.
