Your browser does not fully support modern features. Please upgrade for a smoother experience.
Please note this is an old version of this entry, which may differ significantly from the current revision.
Subjects:
Engineering, Chemical
阿特拉津是一种用于防治禾本科杂草和阔叶杂草的除草剂,已成为农作物保护工具的重要组成部分。它被广泛喷洒在玉米、高粱和甘蔗上,随之而来的问题是其残留在农业食品和洗涤水中。如果摄入人体,这种残留的阿特拉津会导致生殖危害、发育毒性和致癌性。
- atrazine
- degradation
- residue
- agri-food
- water
一、简介
阿特拉津(图 1)是一种应用广泛的三嗪类除草剂,用于控制玉米、甘蔗、高粱和某些其他作物中的禾本科杂草和阔叶杂草 [ 1 , 2 , 3 , 4 ]。由于其效率和成本低,其全球平均消费量为每年 70,000 至 90,000 吨 [ 5 ]。如果购买传统食品,消费者很可能吃过喷洒过阿特拉津的食品。由于阿特拉津被施用于用作牲畜饲料的农作物,其残留物不仅存在于农作物中,还存在于牛奶和肉类中。根据欧洲食品安全局进行的消费者风险评估 [ 6],根据代表 22 个国家饮食的平均消费数据,用于玉米和除玉米以外的其他谷物的膳食慢性暴露计算的阿特拉津输入值分别为 0.025 毫克/千克和 0.05 毫克/千克。虽然不被认为对人有剧毒,但阿特拉津会影响人类的长期健康。阿特拉津可作为内分泌干扰物(EDC)[ 7 ],对内分泌系统产生损害,引起一系列病理变化和生殖异常[ 8 ]。此外,由于对人类健康的负面影响,例如肿瘤、乳腺癌、卵巢癌和子宫癌以及白血病和淋巴瘤,阿特拉津也是一种潜在的致癌物质 [ 9]。由于这些原因,阿特拉津于 2003 年在欧盟 (EU) 被禁用 [ 10 ]。然而,除草剂阿特拉津(如 Gesaprim 90% WG)的商业配方仍广泛用于拉丁美洲。例如,除草剂是 2009 年至 2018 年间巴西使用的主要农药类别,从 52.4%(2011 年)到 62.5%(2012 年)波动,阿特拉津是这一时期的前两种有效成分 [ 11 ]。巴西是世界第三大农产品出口国和拉丁美洲有机食品市场的领导者 [ 12 ]。此外,巴西的主要出口市场是欧盟和美国[ 13]。因此,阿特拉津的残留问题仍然是一个值得关注的问题。阿特拉津化学性质稳定,在水中的半衰期长(30-100 天)[ 14 , 15 ],其在土壤环境中的微生物降解是一个相对缓慢的过程(田间半衰期的范围为 18 至 148 天 [ 16 , 17 ])。它也微溶于水(33 mg·L -1 at 22 °C),在土壤中的吸附性低[ 18 ]。因此,它会污染地表水和地下水[ 19 ]。美国饮用水中阿特拉津的上限为 3 μg/L,而欧洲则固定为 1 μg/L [ 20 , 21 ]。然而,调查 [ 22 ,[ 23 , 24 ] 表明阿特拉津的浓度超过了地表水和地下水中水污染的法定限度。在水中阿特拉津的检测和定量方面已经开展了大量工作 [ 25 , 26 , 27 , 28 ],这对食品安全和质量控制具有重要意义。控制农业食品和洗涤水中残留阿特拉津的污染已成为一个重大问题。
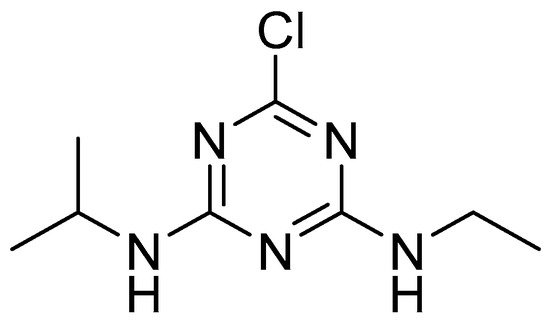
图 1. 阿特拉津(2-氯-4-乙基氨基-6-异丙基氨基-1,3,5-三嗪)。
2. 生物降解
生物降解是指微生物、植物或酶对污染物的部分(有时是全部)转化或解毒[ 118 ]。它在低成本和环境友好方面优于物理和化学方法[ 119 ]。自发现生物阿特拉津降解 [ 120 , 121 ] 以来,生物降解一直是阿特拉津分解代谢的主要方法 [ 1 ]。
2.1。微生物降解
微生物降解利用微生物从污染场地去除污染物的能力[ 122 ]。这是因为已经存在于受污染环境中的本土微生物可能会通过作为其代谢过程一部分发生的反应将污染物转化为无害产品 [ 123 ]。通常,由于污染物的性质和类型,选择分离的微生物进行降解。已分离出不同的阿特拉津降解细菌和真菌(表 5)。由于微生物很容易在水中排出,使其有效性大大降低,Yu 等人。[ 58]开发了一种具有生物吸附和生物降解特性的自固定生物混合物(SIB),可以获得更好的阿特拉津去除率。
表 5. 水性阿特拉津的微生物降解。
| 拉紧 | 起源 | 去除效果 |
|---|---|---|
| 节杆菌 属 DNS10 | 黑土 [ 54 ] | 100 mg/L 阿特拉津在 0.05 mM Zn 2+ 和 1.0 mM Zn 2+中 48 h的去除率分别达到 95% 和 86% [ 55 ]。 |
| 巴氏芽孢杆菌 ABP6 | 玉米田 | Response-surface-methodology (RSM) was used to optimize environmental factors such as pH, temperature, agitation speed and atrazine-concentration on atrazine degradation by utilizing Bacillus badius ABP6 strain. In the optimum conditions (pH 7.05, temperature 30.4 °C, agitation speed 145.7 rpm, and atrazine-concentration 200.9 ppm), the degradation rate of atrazine reaches a maximum value of 90% [56]. |
| Bjerkanderaadusta | Rotten wood surfaces | In the optimum conditions (pH 4, temperature 28 °C, biomass 2 g, and atrazine-concentration 50 ppm), the removal rate of atrazine was up to 92% in 5 days [57]. |
| Agrobacterium sp. WL-1, Arthrobacter sp. ZXY-2 | Jilin Pesticide Plant | After adding biochar ZXY-2 pellets, the removal rate of atrazine reached 61% within 1 h, higher than that treated by ZXY-2 pellets without biochar. The addition of biochar could enhance the connection between ZXY-2 and pellets-based carrier, and the favorable biodegradation pH of ZXY-2 changed to 6 and 10 [58]. |
| Chlorella sp. | The Freshwater Algae Culture Collection at the Institute of Hydrobiology, China | Atrazine with initial concentration of 5 mg/L was photocatalytic degraded for 60 min with degradation ratio of 31%. After an 8 d exposure of the microalga Chlorella sp., 83% and 64% of the atrazine were removed from the degraded solutions containing 40 μg/L and 80 μg/L of atrazine, respectively [124]. |
| Myriophyllum spicatum | Wuhan Botanical Garden | Myriophyllum spicatum absorbed more than 18-fold the amount of atrazine in sediments and degraded atrazine to hydroxyatrazine (HA), deelthylatrazine (DEA), didealkylatrazine (DDA), cyanuric acid (CYA) and biuret. The formation of biuret suggested for the first time, the ring opening of atrazine in an aquatic plant. The residual rate of atrazine was 6.5 ± 2.0% in M. spicatum-grown sediment on day 60 [125]. |
2.2. Phytodegradation
The phytodegradation of organic compounds take place inside the plant or within the rhizosphere of the plant [126]. Rhizosphere, the immediate vicinity of plant roots, is a zone of intense microbial activity, and the use of vegetation at the waste sites can overcome the inherent limitations such as low microbial population or inadequate microbial activity [59]. It has been reported that atrazine can be degraded or detoxified in crops [60,61], and the molecular mechanism for catabolism and detoxification of atrazine in plants is a major research topic (Table 6).
Table 6. Phytodegradation of aqueous atrazine.
| Plant | Gene/Enzymes | Result |
|---|---|---|
| Pennisetum cladestinum | Soil dehydrogenase | Within 80 days, nearly 45% of atrazine was degraded [59]. |
| Rice | Two novel methyltransferases LOC_Os04g09604, LOC_Os11g15040 | Atrazine degradation and detoxification are regulated [62] |
| Alfalfa (Medicago sativa) | Genes encoding glycosyltransferases, glutathione S-transferases or ABC transporters | Atrazine in alfalfa can be detoxified through different pathways [63]. |
Generally, atrazine may be degraded within the plant biomass by plant enzymes as well as in its rhizosphere by microbial biotransformation [127,128].
3. Degradation Pathways, Atrazine Mineralization and Metabolites Toxicity
The degradation of atrazine is a complex process with different pathways through different biotic or abiotic water treatment processes. Regarding the biotic degradation processes, there are two stages [146] (Figure 3). In the first stage, hydrolytic dichlorination and N-dealkylation of atrazine generate cyanuric acid in the role of the enzymes that have broad substrate specificity [147]. For hydrolytic dichlorination of atrazine, enzyme atrazine chlorohydrolase (AtzA) [148] or hydrolase triazine (TrzN) [149] catalyzes hydrolytic dichlorination of atrazine, but they display substantial differences in their substrate ranges: AtzA is restricted to atrazine analogs with a chlorine substituent at carbon 2 and N-alkyl groups, ranging in size from methyl to t-butyl [150], and TrzN hydrolyzes a range of leaving groups (e.g., OCH3, –SCH3, –Cl, –F, –CN) from both triazines and pyrimidines [149]. For N-dealkylation of atrazine, hydroxyatrazine N-ethylaminohydrolase (AtzB) [151] catalyzes the hydrolytic conversion of hydroxyatrazine to N-isopropylammelide, and N-isopropylammelide isopropylaminohydrolas (AtzC) [152] catalyzes the hydrolysis of N-isopropylammelide to cyanuric acid. In the second stage, cyanuric acid is converted to ammonium and carbon dioxide by a set of enzymes AtzDEF [153,154] and TrzD [153,155].
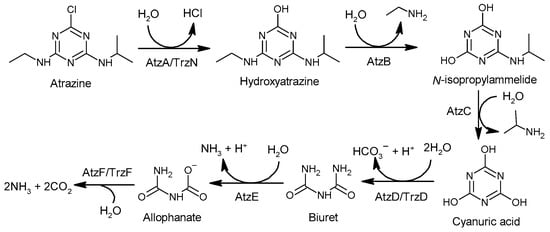
Figure 3. Degradation pathway of atrazine through biotic treatment process.
The above discussion is based on the enzymatic steps catalyzed by the gene products. In actual operation, atrazine degradation may be achieved by a consortium of organisms harboring the appropriate combination of enzymes, for example, the enriched mixed culture as well as the isolated strain, designated as Arthrobacter sp. strain GZK-1, mineralized 14C-ring-labeled atrazine up to 88% to 14CO2 in a liquid culture within 14 d [156].
In addition, for abiotic water treatment processes, as shown in Section 2 and Section 3 of this article, many advanced oxidation processes (AOPs) have been involved in the degradation of atrazine in water. These AOPs can be used individually or in combination to improve efficiency such as US/UV [71,157], US/UV/O3 [114,158], electrochemistry (EC)/O3 [111], UV/H2O2 [159], UV/US/PS [160], UV/MW [161,162], UV/Fenton [83], etc. Generally, AOPs rely on the in situ formation of reactive species [78], such as hydroxyl radical (•OH) [163], sulfate radical (SO4•−) [164,165], singlet oxygen (1O2) [132], superoxide radical anions (O2•−) [37], hydrated electron (eaq−) [78] and hydrogen radical (H•) [78]。这些活性物质具有不同的氧化还原电位和反应选择性。因此,阿特拉津的降解途径因AOP而异。一般涉及的机制是脱氯、s-三嗪环的羟基化、氨基的脱烷基化、氨基的氧化、脱氨基和 s-三嗪环的开环 [ 71 ](图 4) . 在以前的大多数工作中[ 71 , 92 , 114 , 132 , 165 ],阿特拉津降解的最终产物往往是氰尿酸、三聚氰胺和三聚氰胺,因为它很难裂解 s-三嗪环 [ 166 ]。目前,很少有研究[ 45,75 , 81 , 167 , 168 ] 报道了阿特拉津的完全矿化,其中 s-三嗪环裂解产生毒性较小的化合物缩二脲 [ 167 ],缩二脲水解成脲基甲酸酯,最后生成 CO 2 , H 2 O、NH 4 + 和小酸。因此,阿特拉津的完全矿化降低了处理后废水的毒性,以供随后释放。
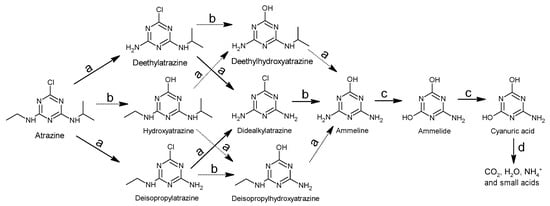
图 4. 一般涉及的阿特拉津降解机制: ( a ) 氨基的脱烷基化;( b ) s-三嗪环的脱氯和羟基化;( c ) 氨基的氧化和脱氨基;( d ) s-三嗪环的开环。
对阿特拉津降解的毒性研究仍然不完整,因为一些阿特拉津代谢物如阿米林缺乏毒理学数据。根据世界卫生组织出版的《食品中农药残留:2007 年毒理学评价》一书[ 169 ],阿特拉津及其氯代三嗪代谢物对雄性大鼠具有中度或低度急性经口毒性(LD 50 ),ATZ、DEA、DIA 和 DDA 分别为 1870–3090、1890、2290 和 3690 mg/kg bw;羟基莠去津对雄性大鼠的急性经口毒性(LD 50,>5050 mg/kg bw)低于莠去津或其氯代代谢物。然而,基于这些 LD 50的毒性比较 数值仍然不准确,因为毒性测试的结果会因不同的受试者(植物、动物、人体细胞等)或不同的关注点(生殖或发育毒性、肝毒性等)而异。更多毒性试验数据见上表(表8)。结合这些数据,大致可以得到如下毒性排名:阿特拉津(ATZ)>去乙基阿特拉津(DEA)>去异丙基阿特拉津(DIA)>三苯丙胺(AM)>双去烷基阿特拉津(DDA)>羟基阿特拉津(HA)。
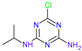
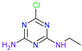
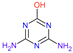
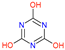
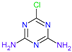
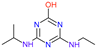
表 8.阿特拉津及其代谢物的化学结构和毒性试验数据。
| 姓名 | 阿特拉津 (ATZ) | Deeth-Ylatrazine (DEA) | 去异丙嗪 (DIA) | 阿米林 (AM) | 三聚氰酸 | Dideal-Kylatrazine (DDA) | 羟基阿特拉津 (HA) |
|---|---|---|---|---|---|---|---|
| 化学结构 | 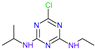 |
 |
 |
 |
 |
 |
 |
| 雄性大鼠的急性经口毒性 (LD 50 ) [ 169 ] | 1870–3090 毫克/公斤 | 1890 毫克/公斤 | 2290 毫克/公斤 | 3690 毫克/公斤 | >5050 毫克/公斤 | ||
| Pseudokirchneriella subcapitata 暴露 96 小时的中位致死浓度 (LC 50 ) [ 170 ] | 1600微克/升 | 2000微克/升 | >3000微克/升 | ||||
| A. variabilis藻类光合作用 50% 的最大影响 (EC 50 ) 的浓度 [ 171 ] | 0.1 ppm | 0.7 ppm | 4.7 ppm | 100 ppm | >100 ppm | ||
| 大鼠急性经口毒性 (LD 50 ) [ 171 ] | >5000 毫克/公斤 | ||||||
| 对绵羊的不良反应 [ 172 ] | 绵羊平均每天摄入 296 mg/kg 体重的 ammeline 42 天,导致半数死亡。 | 在每天 198 至 600 mg/kg 体重的剂量下,77 天没有副作用。 |
不同处理工艺的降解机理、阿特拉津降解率、矿化率和主要产物不同。为了更好地阐述,以下讨论基于处理过程类型。
This entry is adapted from the peer-reviewed paper 10.3390/foods11162416
This entry is offline, you can click here to edit this entry!
